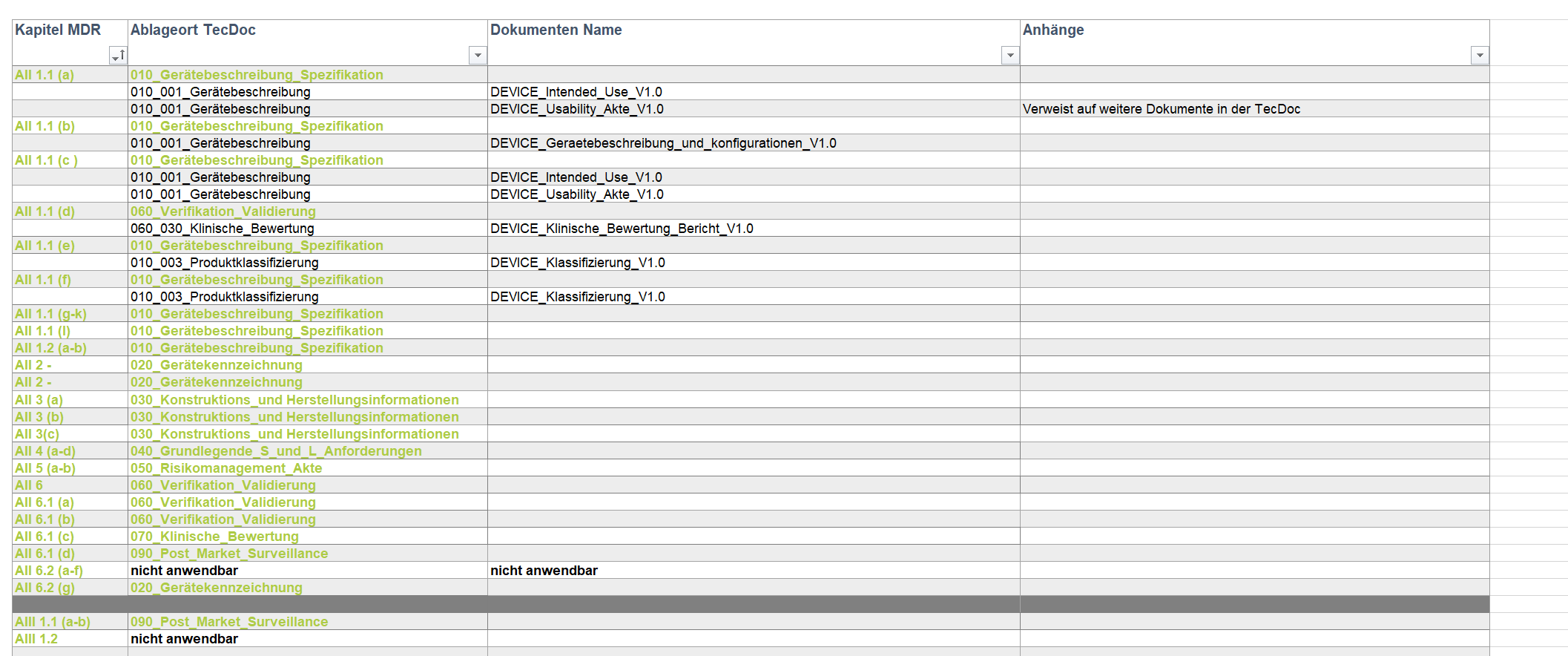
IPP Empfehlung: Inhalt einer Technischen Dokumentation nach MDR, Anhang II & III
In den Anhängen II und III der MDR wird erläutert, was die Technische Dokumentation mindestens beinhalten soll. In Anhang II wird hierbei auf das Produkt selbst eingegangen und Anhang III legt die Anforderungen an die Marktüberwachung nach dem Inverkehrbringen mit Planung und Durchführung fest.