Dr. Volker Klügl
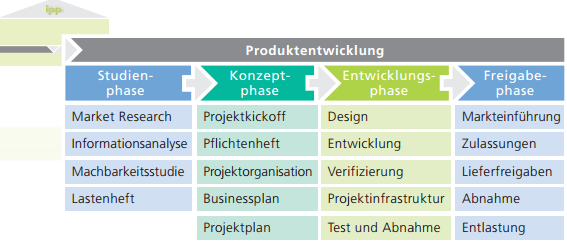
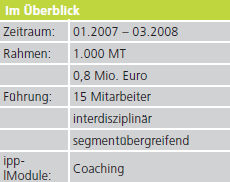
Accelerating Medical Device Market Entry
Managing Director
Dr. Volker Klügl, Beschleunigung des Markteintritts von Medizinprodukten, Minimierung der Lebenszykluskosten durch Management von Ressourcen, Requirements und Regularien.
Dr. Volker Klügl ist Diplom-Ingenieur für Maschinenbau. Er verfügt über mehr als 30 Jahre Berufserfahrung. Bis zu seiner Unternehmensgründung war Dr. Volker Klügl in leitenden Positionen eingesetzt. Durch seine langjährige Tätigkeit als Berater mit dem Schwerpunkt Projektmanagement, ist er Ihr Ansprechpartner, sowohl für das strategisch-konzeptionelle, als auch für das operative Projektmanagement technisch komplexer Projekte. Seit 2005 ist Dr. Volker Klügl Unternehmer und der Inhaber von IPP.
Die Promotion von Dr. Volker Klügl erfolgte in Cardiff, Wales. Im Jahr 1992 fand sein Berufseinstieg im Maschinenbau statt. Anschließend folgte im Jahr 2001 der Wechsel in die Beratung mit dem Schwerpunkt auf dem Projektmanagement. Insbesondere fokussiert er sich seit 2002 auf das Management von komplexen Projekten in der Medizintechnik. Des Weiteren ist Dr. Volker Klügl über die Jahre an den zunehmenden regulatorischen Anforderungen an Klasse 2b Medizinprodukten gewachsen. Seit 2015 konzentriert sich Dr. Volker Klügl auf die Change Management Projekte, die sich aus den aktuellen Herausforderungen aus Digitaler Produktakte, MDSAP, MDR ergeben.
Dr. Volker Klügl ist Ihr Spezialist sowohl für Regulatory Affairs Medizintechnik, technische Dokumentation nach MDR, Regulatory Projektmanagement, Großprojekte, Prozessberatung MDR als auch für Klinische Bewertungen nach MDR am Standort Nürnberg in Bayern.
Veröffentlichungen von Dr. Volker Klügl
- Wellness App oder Medizinprodukt?
- Wann sind Produkte, die die Leistung des menschlichen Körpers messen, noch Wellness-Apps und wann schon Medizinprodukte? Am Beispiel der webbasierten Software Breathment zeigt der Gastbeitrag, wie eine Klassifizierung aussehen kann.
- Aus Sicht neuer Marktteilnehmer: Ist die MDR ein Industriekartell?
- Die MDR ist weiterhin die größte Baustelle in der Medizintechnik-Branche. Noch immer gibt es zu wenig Benannte Stellen, um die Anfragen der Medizinproduktehersteller zu bewältigen und Bestands- sowie Neuprodukte zu zertifizieren. Ist die MDR aus Sicht neuer Marktteilnehmer deshalb ein Industriekartell? Mit dieser Frage setzt sich Dr. Volker Klügl in einem Gastbeitrag auseinander.